Kudosvammaan hakeutuva lääkemolekyyli tehostaa vammojen paranemista

Yksi lääketieteen keskeisistä tavoitteista on nopeuttaa kudosvamman paranemista siten, että vamma-alueelle muodostuisi myös vähemmän toimimatonta arpikudosta. Tampereen yliopiston professori Tero Järvinen johtaa tutkimusta, jossa etsitään ratkaisuja tämän tavoitteen saavuttamiseksi.
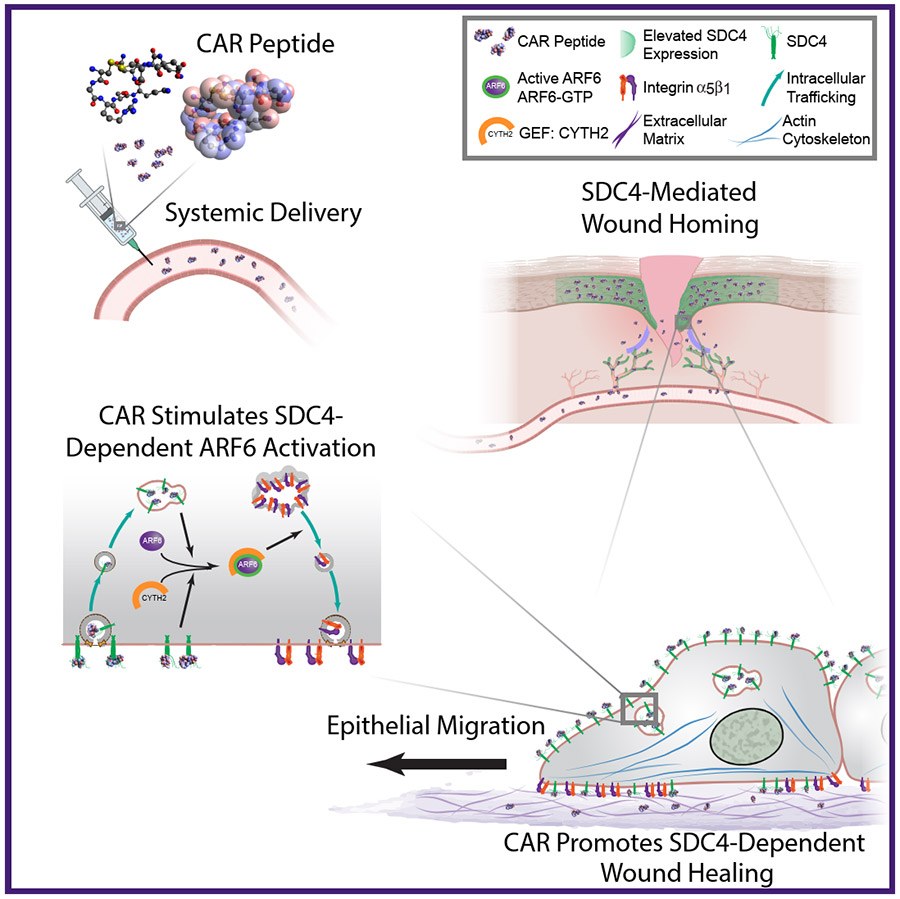
Aikaisemmassa tutkimuksessaan Järvinen löysi niin kutsutun homing peptidin eli pienen proteiinipalasen, joka hakeutuu verenkierron välityksellä spesifisesti kudosvaurioon. Homing peptidi nimettiin aminohappokoostumuksensa mukaan CAR-peptidiksi. Se seulottiin yli miljardin peptidin joukosta. Peptidin avulla pystyttiin kuljettamaan arven muodostumista estävä lääkeaine kohdistetusti kudosvaurioalueelle syntyviin uudissuoniin. Lääkeaine oli annosteltu systeemisesti eli verenkierron kautta.
Nyt tutkimusryhmä osoitti, että CAR-kuljetuspeptidi on itsessään terapeuttinen lääkemolekyyli. Se siis aktivoi ja kiihdyttää haavan paranemista ilman, että siihen liitetään minkäänlaista lääkemolekyyliä.
Tutkimuksessa vahvistettiin, että CAR-peptidi aktivoi haavan paranemiselle kriittisen kudosregeneraatiomekanismin hakeutumalla haavaan verenkierron välityksellä. Haavassa se sitoutui solukalvon reseptoriinsa, syndekaani-4-proteoglykaaniin. Tämä sitoutuminen aktivoi solun sisällä sytohesiini-2-tekijän, joka puolestaan aktivoi Arf6 GTPaasin, joka käynnisti solujen migraation eli vaelluksen kudosvaurioalueen yli.
Tällä mekanismilla CAR-peptidiä saaneiden eläinten ihohaavat sulkeutuivat merkittävästi nopeammin, kuin ne olisivat tehneet ilman hoitoa. Myös arvet jäivät normaalia pienemmiksi.
– Syndekaani-4-riippuvainen kudosregeneraatio on keskeinen tekijä ihohaavojen lisäksi useiden muidenkin kudosvammojen, kuten lihasrepeämien ja luunmurtumien, paranemisessa. Löytämämme peptidi, joka aktivoi tätä luonnon omaa paranemismekanismia, avaa täysin uusia mahdollisuuksia hoitaa vammoja ja tapaturmia. Koska lääkemolekyyli hakeutuu aktiivisesti kudosvaurioon verenkierron välityksellä, vamma voi olla missä tahansa kehon osassa, Järvinen sanoo.
Tutkimus suoritettiin professori Tero Järvisen johdolla ja yhteistyössä akateemikko Erkki Ruoslahden kanssa Tampereen yliopistossa, Sanford Burnham Prebys Medical Discovery Instituutissa (Kalifornia, Yhdysvallat) ja University of California Santa Barbarassa (Kalifornia, Yhdysvallat). Lisäksi tutkimukseen osallistui tutkijoita Liverpoolin yliopistosta ja Manchesterin yliopiston Wellcome Trust Centre for Cell-Matrix Research -keskuksesta.
Tutustu artikkeliin Nature Communications -lehden verkkosivulla