iPS-solut

iPS-solut-palveluyksikkö sijaitsee Arvo-rakennuksessa Tampereen yliopiston Kaupin kampuksella. Yksikkö tarjoaa iPS-soluteknologiaan liittyviä palveluita akateemisille ja ei-akateemisille asiakkaille.
Johdanto
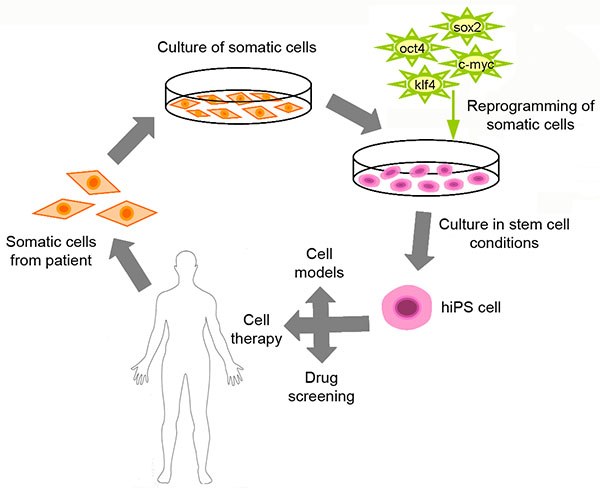
Jo täysin erilaistuneet aikuisen solut voidaan ohjelmoida uudelleen pluripotenteiksi soluiksi määrätyissä olosuhteissa. Uudelleenohjelmoituja soluja kutsutaan indusoiduiksi pluripotenteiksi kantasoluiksi, iPS-soluiksi, ja ne voidaan erilaistaa halutuiksi solutyypeiksi säilyttäen alkuperäinen genotyyppi. Tällä tekniikalla on mahdollista luoda potilaskohtaisia kantasolulinjoja, jotka tarjoavat tavan mallintaa ja tutkia erilaisten ihmissolujen häiriöiden patofysiologiaa. Siksi iPS-soluteknologia tarjoaa lupaavan ja turvallisen alustan potilaskohtaisen lääkehoidon seulomiseen ja optimointiin.
KIITOKSET
Kaikkien näiden palvelujen käyttäjien tulee kiittää iPS-solut-palvelua ja Biocenter Finlandia julkaisuissaan.
“The authors acknowledge the Biocenter Finland and Tampere facility of iPS Cells for the service.”
tai "Kirjoittajat kiittävät Biokeskus Suomea (Biocenter Finland) ja Tampereen iPS-solut-yksikköä palvelustaan."
Biocenter Finland (Biokeskus Suomi) tukee osittain palvelua.

Menetelmät
Olemme optimoineet ei-integratiivisen uudelleenohjelmointimenetelmän iPS-solulaboratoriossamme. iPS-soluja voidaan uudelleenohjelmoida ilman viruksia, episomaalisten vektoreiden avulla, jossa uudelleenohjelmointitekijät viedään soluun elektroporaatiolla. Uudelleenohjelmointi on optimoitu fibroblasteille sekä perifeerisen veren mononukleaarisille soluille (PBMC).
iPS-soluilla on kyky erilaistua kaikkien kolmen alkiokerroksen solu- ja kudostyypeiksi. Määrätyissä olosuhteissa iPS-solut voidaan erilaistaa halutuksi solutyypiksi, kuten sydänlihassoluiksi, hermosoluiksi sekä maksasoluiksi.
iPS-solulaboratoriossa on käytössä automaattisia- sekä puoliautomaattisia menetelmiä, joilla voidaan analysoida sydänsolujen morfologiaa ja toiminnallisuutta. Testeihin kuuluu solujen koon ja orientaation analysointi sekä yksityiskohtaisempi Ca2+ analyysi solujen sähköisen toiminnallisuuden ja sykintäkäyttäytymisen tutkimiseen. Sydänlihassolujen lisäksi näitä määrityksiä voidaan soveltaa moniin muihin solutyyppeihin.
Palvelut
iPS-soluyksikkö tarjoaa seuraavat palvelut:
- Ihmisen iPS-solujen toimittaminen
- Suuri kokoelma tautispesifisiä iPS-soluja sekä terveistä kontrollihenkilöistä peräisin olevia iPS-soluja
- Ihmisen iPS-solujen tuottaminen asiakkaan toimittamista fibroblasteista tai verestä (PBMC)
- Tarvitaan eettisen toimikunnan puoltava lausunto
- Vähintään kahden ihmis- iPS-solukloonin tuottaminen ja peruskarakterisointi
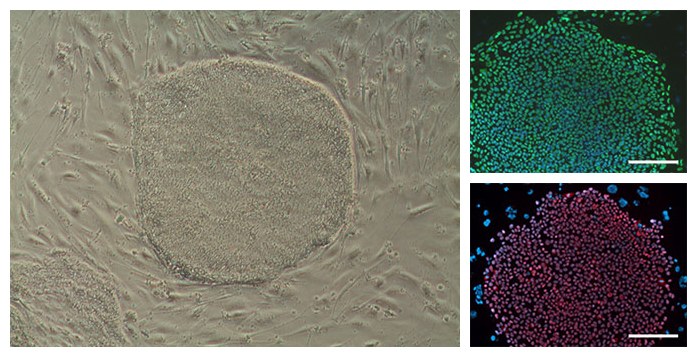
Ihmisen iPS-solujen karakterisointi
- Pluripotenssimarkkereiden karakterisointi (Nanog, Oct4, TRA-1-60, TRA-1-81)
- Endogeenisten ja eksogeenisten markkereiden PCR-analyysi
- In vitro -pluripotenssianalyysi EB:n muodostamisen avulla
- Karyotyyppianalyysi
- Solulinjojen autentikaatio
Ihmisen iPS-solujen erilaistaminen (pyynnöstä)
- Kardiomyosyytit, hepatosyytit
- Erilaistuneiden solujen toimittaminen
- Kardiomyosyytit, hepatosyytit
- Erilaistuneiden solujen karakterisointi
- Optimoidut määritykset erilaistuneiden solujen morfologian (solujen koko ja suuntautuminen) ja toiminnallisuuden (Ca2+-kuvantaminen ja peruselektrofysiologia) sekä sykintäkäyttäytymisen (videoanalyysi) tutkimiseksi
- Testit on optimoitu ihmisen iPS-peräisiä kardiomyosyyttejä varten, mutta samoja menetelmiä voidaan soveltaa myös muille solutyypeille
- Erikoislaitteiden vuokraaminen
- 4D-Nucleofector™ -järjestelmä
- EVOS™ FL Cell Imaging System (DAPI, GFP, RFP)
- Käytännönläheinen koulutus
- iPS Cells -laitos tarjoaa räätälöityä käytännön koulutusta asiakkaille
Hinnat
Valmistamme iPS-solulinjoja pääasiassa perifeerisen verenkierron mononukleaarisista soluista (PBMC) käyttäen nukleofektiota ja plasmidi-vektoreita. Hinta riippuu suuresti projektin yksityiskohdista, siitä kuinka kauan uusia iPS-solulinjoja viljellään sekä siitä, suoritetaanko niille karakterisointia. Ota yhteyttä saadaksesi lisätietoja ja ajantasaiset hintatiedot sekä tiedot ei-akateemisista hinnoista. Alla on arvio iPS-solulinjojen tuottamisen ja karakterisoinnin hinnoista (tilanne 04/2026).
| Tuote | Akateeminen hinta* ei sisällä VAT:ia |
| iPS-solulinjan luominen PBMC:istä** | 1400 € |
| Karakterisoitu iPSC-linja*** | |
| Yksi solulinja | 4800 € |
| Kaksi kloonia samasta näytteestä | 6650 € |
iPS-solujen erilaistaminen Kardiomyosyytit | tiedustele |
| Erilaistuneiden solujen analyysit | tiedustele |
solu koko ja orientaatio Ca2+ -kuvantaminen peruselektrofysiologia mekaaninen liike | |
| Käytännönläheinen koulutus | tiedustele |
| Nucleofector ja EVOS mikroskooppien vuokraaminen | tiedustele |
* pidätämme oikeuden hintojen muutoksiin; ota yhteyttä saadaksesi ajantasaiset hinnat
**sisältää perifeeristen verisolujen (PBMC) eristämisen ja nukleofektion, pesäkkeiden poimimisen (vähintään 6 pesäkettä) sekä soluviljelyn p4-vaiheeseen asti ja pakastamisen (ei karakterisointia)
*** sisältää soluviljelyn p10-vaiheeseen asti sekä karakterisointimääritykset (lisätietoja saatavilla pyynnöstä)
Publications
2022
- Häkli, M, Kreutzer, J, Mäki, AJ, Välimäki, H, Cherian, RM, Kallio, P et al.. Electrophysiological Changes of Human-Induced Pluripotent Stem Cell-Derived Cardiomyocytes during Acute Hypoxia and Reoxygenation. Stem Cells Int. 2022;2022 :9438281. doi: 10.1155/2022/9438281. PubMed PMID:36579142 PubMed Central PMC9792238.
- Le Dour, C, Chatzifrangkeskou, M, Macquart, C, Magiera, MM, Peccate, C, Jouve, C et al.. Actin-microtubule cytoskeletal interplay mediated by MRTF-A/SRF signaling promotes dilated cardiomyopathy caused by LMNA mutations. Nat Commun. 2022;13 (1):7886. doi: 10.1038/s41467-022-35639-x. PubMed PMID:36550158 PubMed Central PMC9780334.
- Prajapati, C, Koivumäki, J, Pekkanen-Mattila, M, Aalto-Setälä, K. Sex differences in heart: from basics to clinics. Eur J Med Res. 2022;27 (1):241. doi: 10.1186/s40001-022-00880-z. PubMed PMID:36352432PubMed Central PMC9647968.
- Rodosthenous, RS, Niemi, MEK, Kallio, L, Perala, M, Terho, P, Knopp, T et al.. Recontacting biobank participants to collect lifestyle, behavioural and cognitive information via online questionnaires: lessons from a pilot study within FinnGen. BMJ Open. 2022;12 (10):e064695. doi: 10.1136/bmjopen-2022-064695. PubMed PMID:36198465 PubMed Central PMC9535212.
- Maria Cherian, R, Prajapati, C, Penttinen, K, Häkli, M, Koivisto, JT, Pekkanen-Mattila, M et al.. Fluorescent hiPSC-derived MYH6-mScarlet cardiomyocytes for real-time tracking, imaging, and cardiotoxicity assays. Cell Biol Toxicol. 2022; :. doi: 10.1007/s10565-022-09742-0. PubMed PMID:35870039 .
- Häkli, M, Jäntti, S, Joki, T, Sukki, L, Tornberg, K, Aalto-Setälä, K et al.. Human Neurons Form Axon-Mediated Functional Connections with Human Cardiomyocytes in Compartmentalized Microfluidic Chip. Int J Mol Sci. 2022;23 (6):. doi: 10.3390/ijms23063148. PubMed PMID:35328569 PubMed Central PMC8955890.
- Gaballah, M, Penttinen, K, Kreutzer, J, Mäki, AJ, Kallio, P, Aalto-Setälä, K et al.. Cardiac Ischemia On-a-Chip: Antiarrhythmic Effect of Levosimendan on Ischemic Human-Induced Pluripotent Stem Cell-Derived Cardiomyocytes. Cells. 2022;11 (6):. doi: 10.3390/cells11061045. PubMed PMID:35326497 PubMed Central PMC8947267.
- Tamlander, M, Mars, N, Pirinen, M, FinnGen, Widén, E, Ripatti, S et al.. Integration of questionnaire-based risk factors improves polygenic risk scores for human coronary heart disease and type 2 diabetes. Commun Biol. 2022;5 (1):158. doi: 10.1038/s42003-021-02996-0. PubMed PMID:35197564 PubMed Central PMC8866413.
- Saari, J, Siddique, F, Korpela, S, Mäntylä, E, Ihalainen, TO, Kaukinen, K et al.. Toward Xeno-Free Differentiation of Human Induced Pluripotent Stem Cell-Derived Small Intestinal Epithelial Cells. Int J Mol Sci. 2022;23 (3):. doi: 10.3390/ijms23031312. PubMed PMID:35163236 PubMed Central PMC8835723.
- Juhola, M, Joutsijoki, H, Penttinen, K, Shah, D, Pölönen, RP, Aalto-Setälä, K et al.. Data analytics for cardiac diseases. Comput Biol Med. 2022;142 :105218. doi: 10.1016/j.compbiomed.2022.105218. PubMed PMID:34999413 .
2021
- Juhola, M, Joutsijoki, H, Penttinen, K, Shah, D, Aalto-Setälä, K. On computational classification of genetic cardiac diseases applying iPSC cardiomyocytes. Comput Methods Programs Biomed. 2021;210 :106367. doi: 10.1016/j.cmpb.2021.106367. PubMed PMID:34474196 .
- Marttila, S, Viiri, LE, Mishra, PP, Kühnel, B, Matias-Garcia, PR, Lyytikäinen, LP et al.. Methylation status of nc886 epiallele reflects periconceptional conditions and is associated with glucose metabolism through nc886 RNAs. Clin Epigenetics. 2021;13 (1):143. doi: 10.1186/s13148-021-01132-3. PubMed PMID:34294131 PubMed Central PMC8296652.
- Häkli, M, Kreutzer, J, Mäki, AJ, Välimäki, H, Lappi, H, Huhtala, H et al.. Human induced pluripotent stem cell-based platform for modeling cardiac ischemia. Sci Rep. 2021;11 (1):4153. doi: 10.1038/s41598-021-83740-w. PubMed PMID:33603154 PubMed Central PMC7893031.
- Prajapati, C, Ojala, M, Lappi, H, Aalto-Setälä, K, Pekkanen-Mattila, M. Electrophysiological evaluation of human induced pluripotent stem cell-derived cardiomyocytes obtained by different methods. Stem Cell Res. 2021;51 :102176. doi: 10.1016/j.scr.2021.102176. PubMed PMID:33485184 .
- Juhola, M, Penttinen, K, Joutsijoki, H, Aalto-Setälä, K. Analysis of Drug Effects on iPSC Cardiomyocytes with Machine Learning. Ann Biomed Eng. 2021;49 (1):129-138. doi: 10.1007/s10439-020-02521-0. PubMed PMID:32367466 PubMed Central PMC7773623.
2020
- Zelnik, ID, Volpert, G, Viiri, LE, Kauhanen, D, Arazi, T, Aalto-Setälä, K et al.. Different rates of flux through the biosynthetic pathway for long-chain versus very-long-chain sphingolipids. J Lipid Res. 2020;61 (10):1341-1346. doi: 10.1194/jlr.RA120000984. PubMed PMID:32651186 PubMed Central PMC7529049.
- Välimäki, H, Hyvärinen, T, Leivo, J, Iftikhar, H, Pekkanen-Mattila, M, Rajan, DK et al.. Covalent immobilization of luminescent oxygen indicators reduces cytotoxicity. Biomed Microdevices. 2020;22 (2):41. doi: 10.1007/s10544-020-00495-3. PubMed PMID:32494857 PubMed Central PMC7270993.
- Shah, D, Prajapati, C, Penttinen, K, Cherian, RM, Koivumäki, JT, Alexanova, A et al.. hiPSC-Derived Cardiomyocyte Model of LQT2 Syndrome Derived from Asymptomatic and Symptomatic Mutation Carriers Reproduces Clinical Differences in Aggregates but Not in Single Cells. Cells. 2020;9 (5):. doi: 10.3390/cells9051153. PubMed PMID:32392813 PubMed Central PMC7290503.
- Juhola, M, Penttinen, K, Joutsijoki, H, Aalto-Setälä, K. Analysis of Drug Effects on iPSC Cardiomyocytes with Machine Learning. Ann Biomed Eng. 2021;49 (1):129-138. doi: 10.1007/s10439-020-02521-0. PubMed PMID:32367466 PubMed Central PMC7773623.
- Heliö, K, Kangas-Kontio, T, Weckström, S, Vanninen, SUM, Aalto-Setälä, K, Alastalo, TP et al.. DSP p.(Thr2104Glnfs*12) variant presents variably with early onset severe arrhythmias and left ventricular cardiomyopathy. BMC Med Genet. 2020;21 (1):19. doi: 10.1186/s12881-020-0955-z. PubMed PMID:32005173 PubMed Central PMC6995042.
- Calejo, MT, Saari, J, Vuorenpää, H, Vuorimaa-Laukkanen, E, Kallio, P, Aalto-Setälä, K et al.. Co-culture of human induced pluripotent stem cell-derived retinal pigment epithelial cells and endothelial cells on double collagen-coated honeycomb films. Acta Biomater. 2020;101 :327-343. doi: 10.1016/j.actbio.2019.11.002. PubMed PMID:31711900 .
- Kreutzer, J, Viehrig, M, Pölönen, RP, Zhao, F, Ojala, M, Aalto-Setälä, K et al.. Pneumatic unidirectional cell stretching device for mechanobiological studies of cardiomyocytes. Biomech Model Mechanobiol. 2020;19 (1):291-303. doi: 10.1007/s10237-019-01211-8. PubMed PMID:31444593 PubMed Central PMC7005075.
2019
- Joutsijoki, H, Penttinen, K, Juhola, M, Aalto-Setälä, K. Separation of HCM and LQT Cardiac Diseases with Machine Learning of Ca2+ Transient Profiles. Methods Inf Med. 2019;58 (4-05):167-178. doi: 10.1055/s-0040-1701484. PubMed PMID:32079026 .
- Calejo, MT, Saari, J, Vuorenpää, H, Vuorimaa-Laukkanen, E, Kallio, P, Aalto-Setälä, K et al.. Co-culture of human induced pluripotent stem cell-derived retinal pigment epithelial cells and endothelial cells on double collagen-coated honeycomb films. Acta Biomater. 2020;101 :327-343. doi: 10.1016/j.actbio.2019.11.002. PubMed PMID:31711900 .
- Kreutzer, J, Viehrig, M, Pölönen, RP, Zhao, F, Ojala, M, Aalto-Setälä, K et al.. Pneumatic unidirectional cell stretching device for mechanobiological studies of cardiomyocytes. Biomech Model Mechanobiol. 2020;19 (1):291-303. doi: 10.1007/s10237-019-01211-8. PubMed PMID:31444593 PubMed Central PMC7005075.
- Kiamehr, M, Klettner, A, Richert, E, Koskela, A, Koistinen, A, Skottman, H et al.. Compromised Barrier Function in Human Induced Pluripotent Stem-Cell-Derived Retinal Pigment Epithelial Cells from Type 2 Diabetic Patients. Int J Mol Sci. 2019;20 (15):. doi: 10.3390/ijms20153773. PubMed PMID:31375001PubMed Central PMC6696227.
- Shah, D, Virtanen, L, Prajapati, C, Kiamehr, M, Gullmets, J, West, G et al.. Modeling of LMNA-Related Dilated Cardiomyopathy Using Human Induced Pluripotent Stem Cells. Cells. 2019;8 (6):. doi: 10.3390/cells8060594. PubMed PMID:31208058 PubMed Central PMC6627421.
- Kiamehr, M, Heiskanen, L, Laufer, T, Düsterloh, A, Kahraman, M, Käkelä, R et al.. Dedifferentiation of Primary Hepatocytes is Accompanied with Reorganization of Lipid Metabolism Indicated by Altered Molecular Lipid and miRNA Profiles. Int J Mol Sci. 2019;20 (12):. doi: 10.3390/ijms20122910. PubMed PMID:31207892 PubMed Central PMC6627955.
- Pekkanen-Mattila, M, Häkli, M, Pölönen, RP, Mansikkala, T, Junnila, A, Talvitie, E et al.. Polyethylene Terephthalate Textiles Enhance the Structural Maturation of Human Induced Pluripotent Stem Cell-Derived Cardiomyocytes. Materials (Basel). 2019;12 (11):. doi: 10.3390/ma12111805. PubMed PMID:31163704 PubMed Central PMC6600740.
- Koivisto, JT, Gering, C, Karvinen, J, Maria Cherian, R, Belay, B, Hyttinen, J et al.. Mechanically Biomimetic Gelatin-Gellan Gum Hydrogels for 3D Culture of Beating Human Cardiomyocytes. ACS Appl Mater Interfaces. 2019;11 (23):20589-20602. doi: 10.1021/acsami.8b22343. PubMed PMID:31120238PubMed Central PMC6750838.
- Kim, J, Shah, D, Potapov, I, Latukka, J, Aalto-Setälä, K, Räsänen, E et al.. Scaling and correlation properties of RR and QT intervals at the cellular level. Sci Rep. 2019;9 (1):3651. doi: 10.1038/s41598-019-40247-9. PubMed PMID:30842620 PubMed Central PMC6403385.
- Viiri, LE, Rantapero, T, Kiamehr, M, Alexanova, A, Oittinen, M, Viiri, K et al.. Extensive reprogramming of the nascent transcriptome during iPSC to hepatocyte differentiation. Sci Rep. 2019;9 (1):3562. doi: 10.1038/s41598-019-39215-0. PubMed PMID:30837492 PubMed Central PMC6401154.
- Jääskeläinen, P, Vangipurapu, J, Raivo, J, Kuulasmaa, T, Heliö, T, Aalto-Setälä, K et al.. Genetic basis and outcome in a nationwide study of Finnish patients with hypertrophic cardiomyopathy. ESC Heart Fail. 2019;6 (2):436-445. doi: 10.1002/ehf2.12420. PubMed PMID:30775854 PubMed Central PMC6437444.
- Kiamehr, M, Alexanova, A, Viiri, LE, Heiskanen, L, Vihervaara, T, Kauhanen, D et al.. hiPSC-derived hepatocytes closely mimic the lipid profile of primary hepatocytes: A future personalised cell model for studying the lipid metabolism of the liver. J Cell Physiol. 2019;234 (4):3744-3761. doi: 10.1002/jcp.27131. PubMed PMID:30146765 .
2018
- Potapov, I, Latukka, J, Kim, J, Luukko, P, Aalto-Setälä, K, Räsänen, E et al.. Information transfer in QT-RR dynamics: Application to QT-correction. Sci Rep. 2018;8 (1):14992. doi: 10.1038/s41598-018-33359-1. PubMed PMID:30301929 PubMed Central PMC6178346.
- Vanninen, SUM, Leivo, K, Seppälä, EH, Aalto-Setälä, K, Pitkänen, O, Suursalmi, P et al.. Heterozygous junctophilin-2 (JPH2) p.(Thr161Lys) is a monogenic cause for HCM with heart failure. PLoS One. 2018;13 (9):e0203422. doi: 10.1371/journal.pone.0203422. PubMed PMID:30235249 PubMed Central PMC6147424.
- Kiamehr, M, Alexanova, A, Viiri, LE, Heiskanen, L, Vihervaara, T, Kauhanen, D et al.. hiPSC-derived hepatocytes closely mimic the lipid profile of primary hepatocytes: A future personalised cell model for studying the lipid metabolism of the liver. J Cell Physiol. 2019;234 (4):3744-3761. doi: 10.1002/jcp.27131. PubMed PMID:30146765 .
- Paci, M, Pölönen, RP, Cori, D, Penttinen, K, Aalto-Setälä, K, Severi, S et al.. Automatic Optimization of an in Silico Model of Human iPSC Derived Cardiomyocytes Recapitulating Calcium Handling Abnormalities. Front Physiol. 2018;9 :709. doi: 10.3389/fphys.2018.00709. PubMed PMID:29997516 PubMed Central PMC6028769.
- Prajapati, C, Pölönen, RP, Aalto-Setälä, K. Simultaneous recordings of action potentials and calcium transients from human induced pluripotent stem cell derived cardiomyocytes. Biol Open. 2018;7 (7):. doi: 10.1242/bio.035030. PubMed PMID:29970475 PubMed Central PMC6078349.
- Juhola, M, Joutsijoki, H, Penttinen, K, Aalto-Setälä, K. Detection of genetic cardiac diseases by Ca2+transient profiles using machine learning methods. Sci Rep. 2018;8 (1):9355. doi: 10.1038/s41598-018-27695-5. PubMed PMID:29921843 PubMed Central PMC6008430.
- Mäki, AJ, Verho, J, Kreutzer, J, Ryynänen, T, Rajan, D, Pekkanen-Mattila, M et al.. A Portable Microscale Cell Culture System with Indirect Temperature Control. SLAS Technol. 2018;23 (6):566-579. doi: 10.1177/2472630318768710. PubMed PMID:29723086 .
- Strässler, ET, Aalto-Setälä, K, Kiamehr, M, Landmesser, U, Kränkel, N. Age Is Relative-Impact of Donor Age on Induced Pluripotent Stem Cell-Derived Cell Functionality. Front Cardiovasc Med. 2018;5 :4. doi: 10.3389/fcvm.2018.00004. PubMed PMID:29423397 PubMed Central PMC5790033.
- Prajapati, C, Ojala, M, Aalto-Setälä, K. Divergent effects of adrenaline in human induced pluripotent stem cell-derived cardiomyocytes obtained from hypertrophic cardiomyopathy. Dis Model Mech. 2018;11 (2):. doi: 10.1242/dmm.032896. PubMed PMID:29361520 PubMed Central PMC5894949.
2017
Kiamehr M, Viiri LE, Vihervaara T, Koistinen KM, Hilvo M, Ekroos K, Käkelä R, Aalto-Setälä K.
Lipidomic profiling of patient-specific iPSC-derived hepatocyte-like cells.
Dis Model Mech. 2017 Sep 1;10(9):1141-1153.
Kuusela J, Larsson K, Shah D, Prajapati C, Aalto-Setälä K.
Low extracellular potassium prolongs repolarization and evokes early afterdepolarization in human induced pluripotent stem cell-derived cardiomyocytes.
Biol Open. 2017 Jun 15;6(6):777-784. doi: 10.1242/bio.024216.
Vuorenpää H, Penttinen K, Heinonen T, Pekkanen-Mattila M, Sarkanen JR, Ylikomi T, Aalto-Setälä K.
Maturation of human pluripotent stem cell derived cardiomyocytes is improved in cardiovascular construct.
Cytotechnology. 2017 Apr 10. doi: 10.1007/s10616-017-0088-1.
2016
Laurila E, Ahola A, Hyttinen J, Aalto-Setälä K.
Methods for in vitro functional analysis of iPSC derived cardiomyocytes – Special focus on analyzing the mechanical beating behavior.
Biochim Biophys Acta. 2016 Jul;1863(7 Pt B):1864-72.
Ojala M, Prajapati C, Pölönen RP, Rajala K, Pekkanen-Mattila M, Rasku J, Larsson K, Aalto-Setälä K.
Mutation-Specific Phenotypes in hiPSC-Derived Cardiomyocytes Carrying Either Myosin-Binding Protein C Or α-Tropomyosin Mutation for Hypertrophic Cardiomyopathy.
Stem Cells Int. 2016;2016:1684792. doi:10.1155/2016/1684792
2015
Juhola M, Penttinen K, Joutsijoki H, Varpa K, Saarikoski J, Rasku J, Siirtola H, Iltanen K, Laurikkala J, Hyyrö H, Hyttinen J, Aalto-Setälä K
Signal analysis and classification methods for the calcium transient data of stem cell-derived cardiomyocytes
Comput Biol Med, 2015, 61:1–7
Kiviaho A, Ahola A, Larsson K, Kujala K, Pekkanen-Mattila M, Venäläinen H, Paavola K, Hyttinen J, Aalto-Setälä, K
Distinct electrophysiological and mechanical beating phenotypes of Long QT syndrome type 1 -specific cardiomyocytes carrying different mutations
IJC Heart & Vasculature, 2015, 8:19-31
Penttinen K, Swan H, Vanninen S, Paavola J, Lahtinen A-M, Kontula K, Aalto-Setälä K
Antiarrhythmic effects of Dantrolene in patients with catecholaminergic polymorphic ventricular tachycardia and replication of the responses using iPSC models
PLoS One, 2015, 10(5):e0135806
Penttinen K, Siirtola H, Ávalos-Salguero J, Vainio T, Juhola M, Aalto-Setälä K
Novel analysis software for detecting and classifying Ca2+ transient abnormalities in stem cell-derived cardiomyocytes
PLoS One, 2015, 10(8):e0135806
Kartasalo K, Pölönen R-P, Ojala M, Rasku J, Lekkala J, Aalto-Setälä K, Kallio P
CytoSpectre: a tool for spectral analysis of oriented structures on cellular and subcellular levels
BMC Bioinformatics, 2015, 16:344
Manzini, S, Viiri L, Marttila S, Aalto-Setälä K
A comparative view on easy to deploy non-integrating methods for patient-specific iPSC production
Stem Cell Rev, 2015, 11(6):900-908
2014
Ahola A, Kiviaho A, Larsson K, Honkanen M, Aalto-Setälä K, Hyttinen J
Video image-based analysis of single human induced pluripotent stem cell derived cardiomyocyte beating dynamics using digital image correlation
Biomed Eng Online, 2014, 13:39
2013
Toivonen S, Ojala M, Hyysalo A, Ilmarinen T, Rajala K, Pekkanen-Mattila M, Äänismaa R, Lundin K, Palgi P, Weltner J, Trokovic R, Silvennoinen O, Skottman H, Narkilahti S, Aalto-Setälä K, Otonkoski T
Comparative analysis of targeted differentiation of hiPSC and hESC reveals variability associated with incomplete transgene silencing in retrovirally derived hiPSC lines
Stem Cells Transl Med, 2013, 2(2):89-93
2012
Lahti A, Kujala V, Chapman H, Koivisto A-P, Pekkanen-Mattila M, Kerkelä E, Hyttinen J, Kontula K, Swan H, Conklin B, Yamanaka S, Silvennoinen O, Aalto-Setälä K
Model for long QT syndrome type 2 using human iPS cells demonstrates arrhythmogenic characteristics in cell culture
Dis Model Mech, 2012, 5(2):220-230
Contacts
Henna Lappi
henna.lappi(at)tuni.fi
Puh: +358 40 190 1786
Huone: ARVO D439
Facility Director:
Katriina Aalto-Setälä, MD
katriina.aalto-setala(at)tuni.fi
Puh: +358 40 582 9567
Huone: ARVO D437